Roteiros Práticos do Passado
__________________________________________
ABALO E TÉTANO - MÚSCULO ERGOGRAFIA
COLETA DE SANGUE DE RATO POR EXSANGUINAÇÃO
CONSUMO DE OXIGÊNIO EM ANIMAIS TERRESTRES
DETERMINAÇÃO DA CONCENTRAÇÃO DE AMÔNIA NA ÁGUA
FISIOLOGIA DO CORAÇÃO MIÔGENICO
FISIOLOGIA DO CORAÇÃO NEUROGÊNICO
REGULAÇÃO DA RESPIRAÇÃO NO CÃO
ESTUDO DO NERVO E DA PLACA MOTORA
PRESSÃO SANGÜÍNEA ARTERIAL NO CÃO
PROPIEDADES FUNCIONAIS DO CORAÇÃO
AÇÃO DA INSULINA EM CAMUNDONGOS
RÃ ESPINHAL E RÃ DESCEREBRADA ESTUDO DOS REFLEXOS
TRANSPORTE ATIVO EM TÚBULO RENAL
VENTILAÇÃO BRANQUIAL EM CRUSTÁCEOS

VENTILAÇÃO BRANQUIAL EM CRUSTÁCIOS
1. OBJETIVOS:
Este estudo objetiva determinar os efeitos da temperatura e das concentrações de oxigênio e gás carbônico na frequência de batimentos do escafognatito do caranguejo Chasmagnathus granulata.
2. MATERIAL:
A) Material biológico:
- Brachyura B) Equipamentos :
- Vidraria comum de laboratório,
- Tubo de oxigênio, -
Água do mar gelada ( 4oC ) e quente ( 40o C )
3. PROCEDIMENTOS:
- Abrir uma pequena janela na região frontal da caraça do animal e observar o escafognatito em funcionamento. Registrar o número de batimentos por minuto. Identificar também os poros inalantes e exalantes.
- Borbulhar CO2 na água soprando por mais ou menos 10 minutos através de uma pipeta e observar possíveis alterações na freqüência dos batimentos no escafognatito.
- Repetir as observações após borbulhar O2 na água e com duas temperaturas diferentes. Cuidado para não causar variações muito bruscas ou muito amplas de temperatura.
- Com base na bibliografia discuta os resultados incluindo uma definição geral de " Q10 " bem como no cálculo de Q10 para o experimento realizado.

TRANSPORTE ATIVO EM TÚBULO RENAL
1. OBJETIVOS:
Determinar a atividade de transporte através dos túbulos renais de peixes, utilizando solução corante e verificar o efeito do cianeto do potássio na difusão renal.
2. MATERIAIS:
A) Material biológico: - Espécime de peixes, preferencialmente marinho.
B) Reagentes e equipamentos:
- Solução fisiológica.
- Solução de vermelho fenol 2,5 mg/100ml solução fisiológica.
- Solução KCN 50 mg/100ml solução fisiológica.
- Microscópio.
- Material de dissecação.
- Vidraria comum de laboratório.
3. PROCEDIMENTOS:
- Mate o peixe seccionando a medula dorsal na altura da abertura opercular.
- Disseque os rins, situado na parte dorsal da cavidade corpórea e coloque-os em uma placa de Petry contendo solução fisiológica previamente arejada e resfriada.
- Com uma tesoura fina corte os rins em pedaços pequenos e, com o auxílio de uma pequena pinça e estilete pontiagudo ou bisturi, separe os pedaços até que os fragmentos tenham menos de 1 mm de diâmetro.
- Coloque na depressão de 3 lâminas escavadas as soluções abaixo indicadas e 2 ou 3 pequenos fragmentos de tubulos renais em cada uma:
1a. Lâmina: 4 gotas de solução fisiológica
2a. Lâmina: 4 gotas de solução de vermelho fenol
3a. Lâmina: 2 gotas de solução de KCN e 2 gotas de solução de vermelho fenol
- Examine os tecidos ao microscópio no início do experimento em 5, 10, 20, 30 e 60 minutos após o início do experimento. Registre as concentrações de corante nas células (se possível), na luz do ducto ou ambas com uma escala arbitrária desde "mínima" ( + ) até "máxima" ( ++++ ).
- Discuta os resultados e a ação do KCN. Se o trabalho estiver sendo feito com peixe marinho leve em consideração que este possui praticamente só túbulo proximal. No peixe de água doce apenas cerca de 10% do túbulo é proximal.
ATENÇÃO: NÃO PIPETE A SOLUÇÃO DE KCN . EVITE QUALQUER CONTATO DIRETO COM ESTA SUBSTÂNCIA.

RÃ ESPINHAL E RÃ DESCEREBRADA ESTUDO DOS REFLEXOS
INTRODUÇÃO:
Os sentidos somáticos são mecanismos nervosos que coletam informações sensoriais, a partir da estimulação de receptores especiais espalhados por todo o corpo do organismo. Quase todas as informações sensoriais dos segmentos somáticos se dirigem para a medula espinhal e atingem o tálamo e as regiões superiores do córtex cerebral. Algumas sensações podem ser percebidas a nível medular e nas regiões inferiores do cérebro.
OBJETIVOS:
Verificar os reflexos da rã com os hemisférios cerebrais, encéfalo e medula destruídos, comparando com os comportamentos emitidos pela rã íntegra. Identificar as leis de reflexo.
Equipamentos:
-Bacia
-Beckers pequenos
-Gase
-Haste metálica com gancho
-Material de dissecação
Material Biológico:
Rana catesbiana
Reagentes e Soluções:
Água destilada
Ácido Acético Glacial
Ácido Acético 2,0 %
Soluções para os estímulos químicos:
| SOLUÇÕES | CONCENTRAÇÃO FINAL |
| 5 cm3 de solução a 2% + 45 cm3 de H2O | = 1 / 500. |
| 5 cm3 de solução a 2% + 40 cm3 de H2O | = 1 / 450. |
| 5 cm3 de solução a 2% + 35 cm3 de H2O | = 1 /400. |
| 5 cm3 de solução a 2% + 30 cm3 de H2O | = 1 / 350. |
| 5 cm3 de solução a 2% + 25 cm3 de H2O | = 1 / 300. |
| 5 cm3 de solução a 2% + 20 cm3 de H2O | = 1 / 250. |
| 5 cm3 de solução a 2% + 15 cm3 de H2O | = 1 / 200. |
| 5 cm3 de solução a 2% + 10 cm3 de H2O | = 1 / 150. |
| 5 cm3 de solução a 2% + 05 cm3 de H2O | = 1 / 100. |
PROCEDIMENTOS:
1 a Etapa:
Preparação do animal Os animais são previamente anestesiados com Éter de Petróleo, via aérea, em câmara fechada. O professor responsável pela prática realiza a preparação da rã descerebrada e da rã espinhal.
1- Rã descerebrada:
Seguindo uma linha imaginária tangente aos bordos anteriores das duas membranas timpânicas, pratica-se por meio de um bisturi uma incisão transversal na parte superior da cabeça. Pela fenda operatória introduz-se um estilete e destroem-se os hemisférios cerebrais. Abandona-se o animal durante algum tempo, para que se refaça o traumatismo.
2- Rã espinhal:
Com o mesmo animal faz-se uma incisão tomando como ponto de referência os bordos posteriores das manchas timpânicas. Pela ferida introduz-se um estilete e destrói-se cuidadosamente o encéfalo, deslocando alternativamente a agulha para um lado e outro, respeitando a medula espinhal.
2 a Etapa: Procedimentos Experimentais
1- Rã normal: Observar na rã íntegra a postura, equilíbrio, comportamentos sexuais, de fuga e frequência respiratória. Observar o nado do animal.
2- Rã descerebrada: Compara os comportamentos da rã íntegra com os da rã que teve seus hemisférios cerebrais destruídos.
Como está a frequência respiratória? Discuta o porquê.
Quais os comportamentos são mantidos e por que?
3- Rã espinhal: Faça as mesmas observações para a rã que teve o encéfalo destruído. Quais são as diferenças observadas e por que elas ocorrem?
3 a Etapa: Verificação da Leis dos Reflexos. Utilizar a rã espinhal. Enxugar o animal. Pendurar a rã na haste metálica pela região anterior. Estimular quimicamente uma das patas da rã utilizando solução de ácido acético a 2 % (da mais fraca para a mais forte). As soluções de ácido serão colocadas em pequenos beckers devidamente identificados.
Estimula-se apenas uma das patas. Os estímulos não deverão exceder 30 seg e deverão ser sempre aplicados na mesma pata. Retirar o ácido e observar o animal. Entre um estímulo e outro, o animal deverá ser lavado e enxugado. Embeber com ácido acético puro um pedaço de papel e colocar com pinça na parte dorsal ou ventral do animal.
Observar a reação reflexa.
Observar e conceituar as seguintes leis dos reflexos:
Lei da localização.
Lei da unilateralidade.
Lei da simetria.
Lei da irradiação.
Lei da generalização.
4 a Etapa:
Destruição da Medula Espinhal. Introduzir o estilete pela ferida existente no bordo posterior das manchas timpânicas e destruir a medula. Observar quais os comportamentos são emitidos.
CONCLUSÕES: Discutir os resultados e a importância dos vários reflexos observados.
VOCÊ PODE SOLICITAR A VÍDEO AULA.

ENZIMAS DIGESTIVAS
Objetivos:
Determinar a existência de proteases, lipase e amilase na saliva humana e no extrato de estilete cristalino de bivalve ou no suco digestivo de crustáceo.
Material biológico:
Mesodesma mactroides (ou outro bivalve); ou o caranguejo Neohelice granulata.
Material procedimental:
| Água do mar filtrada | Solução de benedict |
| Solução de amido a 1% | Bico de Bunsen |
| Óleo de oliva | Material de dissecação |
|
Chapas veladas de filme fotográfico |
Vidraria comum de laboratório |
| Solução fenolftaleína | Solução lipase pancreática |
|
Solução de NaOH 0,5 g/1000 ml H2O |
Solução tripsina |
Procedimentos:
A) Preparo de extratos.
• Estilete cristalino: Retire 4 estiletes cristalinos de bivalves e, após cortá-los em pequenos pedaços, macere-os em um gral resfriado com 1,0 ml de água do mar. Após macerado adicione mais 1ml de água do mar.
• Solução amilase: Após lavar bem a boca com água destilada cuspir em tubo de ensaio . Diluir na proporção de 3:1 com água destilada. • Retirar com o auxílio de uma seringa, introduzida entre as peças bucais de N. granulata, uma amostra do suco digestivo.
• Bile - utilizar bile de cão.
B) Teste de amilase.
Monte e rotule 3 tubos de ensaio com as seguintes substâncias:
•Tubo 1: 1 ml de solução de amido.
•Tubo 2: 1 ml da solução de amido mais 1 ml de amilase.
•Tubo 3: 1 ml de solução de amido mais 1 ml de extrato de estilete cristalino ou de suco digestivo de crustáceo.
Após uma hora verificar a presença de açúcar (neste caso maltose) com reativo de Benedict. Para tanto, colocar em um pequeno tubo de ensaio 2 gotas de substância ou mistura a ser testada , 8 gotas de água e 4 gotas de reativo de benedict. Aqueça por 10 minutos em banho-maria . A formação de um precipitado vermelho indica resultado positivo.
C) Teste de Lipase.
Monte e rotule 3 tubos de ensaio com as seguintes substâncias:
•Tubo 1 - 1 ml de óleo de oliva mais 2 gotas de bile, 4 gotas de fenolftaleína
•Tubo2 - 1 ml de óleo de oliva mais 2 gotas de bile, 1 ml de solução lipase pancreática mais 4 gotas de fenolftaleína.
•Tubo 3 - 1 ml de óleo de oliva mais 2 gotas de bile, 1 ml de extrato de estilete cristalino/ ou suco digestivo de crustáceo, mais 4 gotas de fenolftleína. O pH das misturas deve ser básico, para tanto verifique se a fenolftaleína deu a solução uma coloração rósea. Atenção, pois a cor fica um tanto mascarada pelo verde da bile. Caso negativo adicione solução de NaOH, gota a gota, até que a mistura adquira uma tonalidade rósea. Verifique se o tom róseo se mantém após 1 ou 2 horas, resultado negativo indica a presença de lipase.
D) Teste de protease.
Goteje sobre a superfície gelatinosa de um filme fotográfico velado e seco algumas gotas das seguintes misturas:
- Solução de tripsina - Extrato de estilete cristalino ou suco digestivo de crustáceo
- Água do mar.
Coloque os filmes em uma placa de petry com papel de filtro umedecido e deixe numa estufa a 37oC por 1 ou 2 horas. Lave o filme se a gelatina tiver sido digerida, as partículas de prata do filme sairão e deixarão uma mancha clara.

AÇÃO DA INSULINA EM CAMUNDONGOS
Introdução:
A insulina é um hormônio anabólico sintetizado no pâncreas, sendo o hormônio mais importante na regulação do metabolismo energético. Sua principal função é regular o metabolismo da glicose por todos os tecidos do corpo, com exceção do cérebro. Ela aumenta a velocidade de transporte da glicose para dentro das células musculares e do tecido adiposo. Com a captação da glicose, se ela não for imediatamente catabolizada como fonte de obtenção energética, gera-se glicogênio nos músculos e triglicerídeos no tecido adiposo. Ou seja, o efeito da insulina é hipoglicemiante, visto que reduz a glicemia sangüínea.
Objetivos:
Esta prática visa demonstrar o efeito da ação da insulina em camundongos, enfocando a importância deste hormônio na absorção de glicose pelas células.
Material biológico:
- 6 camundongos (21-30 dias)
Material procedimental:
| Insulina | Agulhas |
| Glicose 20% | Banho-maria à 37°C (1) |
| Álcool etílico | Termômetros |
| Algodão | Pinça longa |
| Luvas | Becker pequeno |
| Seringas (1 ml) | Gaze |
| Conta-gotas |
|
Banho maria para camundongos |
Procedimentos:
1.Injeção de insulina:
1.1. Injetar insulina intraperitonialmente nos camundongos cada um com uma das seguintes dosagens: 0,25, 0,5, 0,7 e 1,0 ml de insulina
1.2. Colocar os camundongos no banho-maria a 37°C e aguardar a ação da insulina Comparar se o efeito da insulina é dose dependente
2.Teste dos efeitos da insulina
Quando o camundongo estiver letárgico, retire-o do banho com o auxílio de uma pinça e após segurando-o pela cauda, faça alguns movimentos giratórios e coloque o animal sobre a mesa.
Observe se o animal emite comportamento convulsivo.
3.Reversão dos efeitos da insulina
3.1 Após observar as convulsões do camundongo injete glicose subcutânea no dorso do animal e aguarde a recuperação.
Discussão sugerida:
Procure as seguintes questões:
1.Qual o efeito da injeção de insulina no camundongo?
2.Por que o animal apresenta letargia e comportamentos convulsivos?
3.Por que a glicose consegue inibir os efeitos da insulina?

DUODENO ISOLADO DE COELHO
Material biológico:
-duodeno de coelho
Material procedimental:
| Tyrode | Material cirúrgico |
| Oxigênio | Quimógrafo e acessórios (1.1 e 1.2) |
| Acetilcolina (5mg/ml) | Banho-maria (2) para órgão isolado |
| Adrenalina (1:10) |
Procedimentos iniciais:
Procurar inicialmente, familiarizar-se com a operação do aparelho para órgão isolado. Verificar, especialmente, como se enche e se enxazia o banho para órgão isolado.
→ Regular o borbulhamento do oxigênio
→ Regular a temperatura do banho em torno de 38°C
→ Tomar uma porção do duodeno e amarrar as extremidades com fios longos.
→ Amarrar um dos fios ao suporte de vidro que deve ser mergulhado no banho e prender o outro a alavanca de inscrição frontal.
→ Adaptar a alavanca na superfície do tambor do quimógrafo, de maneira a ficar perfeitamente frontal.
OBS: Manusear o órgão isolado o mínimo possível com metais e com as mãos.
|
Cilindro Esfumaçado |
Suporte do Quimógrafo |
|
Banho Maria |
Banho Maria Completo |
|
Lâmpada para Banho Maria |
Procedimentos experimentais:
1.Registrar a atividade normal do intestino com o banho a 38°C e oxigenado.
2.Goteje diretamente sobre o intestino: a)Acetilcolina: registre o efeito, lave a preparação, esvaziando e enchendo com o tyrode, restabelecendo as condições. b)Adrenalina: registre o efeito e repita a operação de lavagem. c)Atropina: registre o efeito e repita a operação de lavagem.
3.Trocar o banho para 10°C. a)Registrar os efeitos novamente e restabelecer as condições iniciais com tyrode a 38°C e registrar novamente.
4.Provocar anoxia: fechar a entrada de oxigênio por um minuto sem registrar. Após este período registrar mantendo a anoxia, durante um minuto.
5.Restabelecer a oxigenação e registrar as condições iniciais.

PROPIEDADES FUNCIONAIS DO CORAÇÃO
INTRODUÇÃO:
A fisiologia cardiovascular estuda a interação entre o sistema circulatório e o coração. O coração é uma bomba que dá ao sangue o fluxo necessário para que ocorra fluxo. Podemos considerar a existência de dois corações, um direito composto pelo átrio e ventrículo direito, que bombeia sangue para os pulmões (circulação pulmonar), e o coração esquerdo, composto pelo átrio e ventrículo esquerdo, que bombeiam sangue para a circulação sistêmica. O músculo cardíaco, por sua vez, também pode ser considerado com músculo atrial e músculo ventricular, já que estão separados por um septo de tecido fibroso. O miocárdio como um todo apresenta características similares às do músculo esquelético e outras características peculiares, como automatismo e atividade sincicial.
OBJETIVO:
Serão estudados, no coração da rã (Rana cateisbiana), alguns aspectos das quatro propriedades fundamentais do miocárdio: automatismo, excitabilidade, condutibilidade e contractilidade.
MATERIAIS
- Rã
- Tesoura de ponta fina
- Estilete
- Prancha de parafina
- Barbante
PROCEDIMENTO CIRÚRGICO:
Imobilizar a rã.
Com uma tesoura de ponta fina cortar a pele sobre a cabeça. Encaixar o estilete na região entre a porção posterior do crânio e o início da coluna vertebral (procurar um "v" sobre a cabeça da rã) e introduzi-lo em direção ao cérebro.
Fazer o mesmo em direção a medula destruindo o sistema nervoso central. Fixar o animal na prancha em decúbito ventral.
Desarticular com tesoura a escápula, corte e rebata primeiro a pele e depois corte a musculatura contornando o osso supra escapular.
Isole o nervo vago com cuidado, com barbante amarrando longe do nervo. (Procure um nervo que corre na axila perpendicular ao plexo braquial que enerva o membro anterior).
Com o animal em decúbito dorsal, abrir o tórax (primeiro a pele, e depois a musculatura contornando o osso externo) extirpando o externo e cortando suas conexões com as clavículas (use a tesoura maior).
Expor o coração, seccionando cuidadosamente, o pericárdio.
Importante: não manuseie o coração com instrumentos metálicos, pois isto pode provocar despolarização nas fibras musculares
OBSERVAÇÕES PRELIMINARES
1- Observe os batimentos do coração em sua posição normal. - Identifique as câmaras cardíacas.
2- Rebata o coração em direção a região anterior do corpo. Manuseie o mínimo possível. - Qual é a seqüência das contrações?
PROCEDIMENTOS EXPERIMENTAIS
1- Zona de Automatismo: tem a capacidade celular de gerar estímulos. A zona de automatismo possui frequência mais alta, passa a comandar a ativação cardíaca submetendo a excitação de todas as fibras ao seu próprio ritmo. Torna-se assim, o marca-passo cardíaco propriamente dito. A frequência das zonas de marca-passo pode ser alterada por modificações das concentrações de íons, temperatura e especialmente pelo sistem a neurovegetativo (adrenalina e acetilcolina ).Identifique o marca-passo cardíaco do coração da rã. (Para tanto observe cuidadosamente a sequência de batimentos).
2- Excitabilidade: É a propriedade que tem o miocárdio de reagir (potencial de ação e contração) quando estimulado. Fixar o coração ao sistema de registro do quimógrafo. Prender um alfinete em "S " no ápice de ventrículo. Cuidado para não perfurar a cavidade ventricular. Certifique-se de que a pena utilizada para o registro tenha uma boa excursão pelo quimógrafo, fazendo um registro normal da atividade, durante 30 segundos, em velocidade alta.
2.1. Observe a atividade sincicial do músculo cardíaco.
2.2. Efeito da temperatura e do sistemas simpático e parassimpático.
2.2.1. Goteje a solução Ringer a 25°C sobre o coração. Observe a frequência e amplitude da atividade cardíaca.
2.2.2. Estímulos elétricos - Com a rã em decúbito dorsal, um aluno deverá segurar a pata dianteira da mesma, enquanto outro irá estimular o vago já isolado, com a caneta do estimulador. Para isso peça ajuda ao professor.
Observe a alteração na frequência. Observe escape vagal ou ventricular.
Utilize a caneta do estimulador para provocar estímulos elétricos direcionados sobre o ventrículo da rã. Faça estímulos no final da diástole e no final da sístole ventricular.
Observe o fenômeno de extrassístoles.
Em qual das fases ocorreram extrassístoles? Observe a pausa compensatória, por que ela ocorre?
OBS. Não realize estímulos demorados, porque este é um coração de verdade e você pode acabar provocando um anfibiocídio.
2.2.3. Estímulos químicos:
Coloque 3 gotas de adrenalina (1:1000). Observe a freqüência cardíaca após cada estímulo.
Faça o mesmo com 3 gotas de acetilcolina (0,1%). Faça o mesmo com 3 gotas de atropina (1 mg/ml) + 3 gotas de aceti lcolina. Faça o mesmo com 3 gotas de atropina e após aplique estímulo no vago.
OBS. Sempre banhar o coração com Ringer entre as etapas.
3. Condutibilidade:
Capacidade que as fibras cardíacas têm de conduzir o estímulo gerado em uma parte do coração para todo o resto do miocárdio.
3.1. Primeira Ligadura: Passe um fio grosso entre o ventrículo e os átrios O que ocorre com o batimento das cavidades?
4. Contractilidade:
É a propriedade que tem o miocárdio de contrair-se, funcionando o coração como um sincício. Ele responde segundo a lei do tudo-ou-nada (ou responde com uma contração total ou não responde).
4.1. Constate a Lei do Tudo ou Nada: Com a ligadura entre os átrios e o ventrículo, com este parado, aplique estímulos isolados e graduais no miocárdio ventricular, até obter resposta.
O que ocorre com atividade ventricular?
Qual a diferença em aplicar um estímulo de baixa ou alta voltagem?
4.2. Segunda Ligadura: Não desfaça o primeiro bloqueio e coloque agora outra ligadura entre o seio venoso e os átrios. O que ocorre com o batimento das cavidades cardíacas ?
RECOMENDAÇÕES FINAIS
Para cada assunto a ser observado você encontra perguntas em azul que direcionam as suas observações; procure responde-las, observando minuciosamente os comportamentos emitidos pelo músculo cardíaco, anotando e discutindo os resultados.

PRESSÃO SANGÜÍNEA ARTERIAL NO CÃO
1. PROCEDIMENTOS PRELIMINARES:
1. Pesar o cão e anestesiá-lo com pento barbital sódico intravenoso (30 mg/kg) ou tio nembutal (30 mg/kg ) – injetar lentamente.
2. Inserir uma cânula na traquéia.
3. Dissecar as veias e artérias femurais, os nervos vagos e as artérias carótidas comuns (de ambos os lados).
4. Montar o registro da pressão da artéria femural de um lado (expor 5 cm da artéria, ligando os ramos colaterais dessa região e introduzir na artéria uma cânula ligada ao manômetro de mercúrio).
5. Registrar a pressão arterial durante 40 segundos antes e depois de cada experiência, o que servirá de controle.
6. Contar o número de batimentos do coração antes e no decorrer de cada experiência.
2. PROCEDIMENTO EXPERIMENTAL:
A. Efeitos da Pressão Pleural Alta (Experiência de Valsalva):
Ao final de uma inspiração, obstruir a traquéia e aplicar forte pressão manual sobre o tórax, durante 30 a 60 segundos e observar os efeitos.
B. Efeitos da Adrenalina:
Injetar rapidamente na veia femural (usar a veia do lado oposto em que está sendo registrada a pressão) adrenalina 100 mg/ml. Observar os efeitos. Aguardar a normalização da pressão.
C. Efeitos da Acetilcolina:
Injetar acetilcolina (100 mg/ml) na veia femural. O coração deverá tornar-se mais lento e a pressão arterial cairá. Se não obtiver resultados, repetir a injeção com dose três vezes maior. Aguardar a normalização da pressão.
D. Efeito da Oclusão das Carótidas Comuns:
Faça o registro controle. Com a pinça arterial ocluir a carótida esquerda durante 1 minuto. Observar o efeito. Com a carótida esquerda ainda ocluída, pinçar a carótida direita. Observar o efeito. Retirar a pinça da carótida direita (mantendo-se o pinçamento da esquerda, observar o efeito por 2 minutos). Retirar a pinça da carótida esquerda e observar o efeito. Aguardar a normalização da pressão.
E. Efeito da Estimulação do Vago Esquerdo:
Registre o traçado controle, e em rápida sequência, ligue o vago esquerdo, seccionando-se em seguida – a secção deve ser tal que deixe as porções cefálica e periférica com dimensões que possam ser estimuladas. Estimulação da Porção Caudal – 50 Hz, 2ms e 15 volts durante 1 minuto.
F. Efeitos da Atropina:
Injetar atropina na veia femural. Depois de 1 a 2 minutos anotar os efeitos sobre o número de batimentos cardíacos e a pressão arterial. Repetir a injeção de acetilcolina e adrenalina como nos ítens B e C.
G. Fibrilação Ventricular:
Aplicar uma corrente elétrica de alta voltagem sobre o miocárdio. Observar o coração e a pressão. Que coloração apresentam as aurículas depois da fibrilação?
3. RESULTADOS
| Tipo de experiência | Freq.card.(bat./min) | Pressão arterial (mm Hg) |
| A. Experiência de Valsalva | ||
| Controle | ||
| Pressão pleural aumentada | ||
| B. Adrenalina | ||
| Controle | ||
| Após injeção de adrenalina | ||
| C. Acetilcolina | ||
| Controle | ||
| Após injeção de acetilcolina | ||
| D. Pinçamento das carótidas | ||
| Carótida esquerda | ||
| controle | ||
| pinçamento | ||
| Carótida direita | ||
| Controle | ||
| Pinçamento | ||
| Retirar a pinça da carót. dir. | ||
| E. Estimulação do vago | ||
| Controle | ||
| Secção do vago | ||
| Estímulo da porção caudal | ||
| F. Atropina | ||
| Controle | ||
| Após injeção de atropina | ||
| Após injeção de acetilcolina | ||
| Após injeção de adrenalina | ||
| G. Fibrilação Ventricular | ||
| Controle | ||
| Após fibrilação | ||
| Após desfibrilação |

MUDANÇA DE COR FISIOLOGICA
INTRODUÇÃO:
A mudança de cor fisiológica aparece em alguns invertebrados, como cefalópodes e crustáceos e nos vertebrados pecilotérmicos; nestes dois últimos baseia-se na migração de grânulos dentro do cromatóforo. Essas adaptações são rápidas, completando-se em segundos ou minutos. O animal clareia quando os grânulos de cromatóforos escuros (melanóforos e eritróforos) se agregam no corpo celular, deixando as projeções celulares vazias de pigmento, enquanto os grânulos de cromatóforos claros (xantóforos e leucóforos) se dispersam pelas projeções. Quando o animal escurece, melanóforos e eritróforos apresentam o pigmento disperso e xantóforos e leucóforos, o pigmento agregado. Os mecanismos para mudança de cor fisiológica são extremamente complexos. Desaparecem nas aves e mamíferos, que apresentam apenas a mudança de cor morfológica.
1. OBJETIVOS:
Reconhecer cromatóforos, seus índices de dispersão e determinar] os efeitos de alguns neurotransmissores e bloqueadores.
2. MATERIAL:
A) Material biológico:
- Escamas de peixe.
B) Reagentes e equipamentos:
- Adrenalina = 0,3 mg/ml em solução fisiológica;
- Solução fisiológica; - Solução de beta-bloqueador;
- Solução de alfa-bloqueador;
- Microscópio;
- Papel de filtro;
- Vidraria comum de laboratório.
3. PROCEDIMENTOS:
- Colocar uma ou duas escamas de peixe em 3 lâminas escavadas, com um pouco de solução fisiológica e levar ao microscópio.
- Fazer um esquema e identificar os diferentes tipos de cromatóforos. - Enquadrar os melanóforos na escala de 1 a 5 (HOAR, 1975, pág. 630).
- Feito isso, procurar em cada uma das lâminas uma região com os melanóforos bem dispersos (índice de 4 a 5).
* Lâmina 1: Substituir a solução fisiológica por solução de adrenalina.
* Lâmina 2: Substituir a solução fisiológica por solução de beta-bloqueador. Após dois minutos, trocar por adrenalina.
* Lâmina 3: Substituir a solução fisiológica por solução de alfa-bloqueador. Após dois minutos, trocar por adrenalina.
- Observar e desenhar.
- Anotar a temperatura.
4. COM BASE NA BIBLIOGRAFIA DISCUTir OS RESULTADOS
Que sistemas estão envolvidos normalmente no controle da mudança de cor em peixes? Descreva-os.

SISTEMA SENSORIAL
1.Introdução:
A maioria das atividades do sistema nervoso é iniciada pela experiência sensorial que emana dos receptores sensoriais, quer sejam visuais, auditivos, táteis ou de outros tipos de receptores. A experiência sensorial pode causar uma reação imediata, ou sua memória pode ser armazenada no cérebro por minutos, semanas ou anos, vindo posteriormente auxiliar na emissão de respostas aos mesmos estímulos. A porção somática do sistema sensorial transmite as informações sensoriais dos receptores vindas de todas as partes do corpo. Estas informações entram no sistema nervoso via nervos periféricos e são conduzidas para áreas sensoriais múltiplas na medula espinhal, na substância reticular da ponte, bulbo e do mesencéfalo, no cerebelo, no tálamo e nas áreas somestésicas do córtex cerebral.
2.Objetivo:
Estudar os receptores periféricos e suas propriedades.
3. Materiais Equipamentos:
Material Biológico:
-Agulhas hipodérmicas (1, abaixo; 2; 3)
-Algodão Bacias (2)
-Beckers pequenos (2; 3)
-Canetas de cores diferentes
-Compasso (2; 3)
-Bandeja
-Pêlo Excitador de U. Frey (1, acima 2; 3; 4.1 e 4.2)
-Régua (2; 3)
-Relógio com ponteiro marcando os segundos
-Termômetro (2;3)
|
1- Pêlo de U.Frey e agulha hipodérmica |
2- Aula sistema sensorial |
|
2b- Aula sistema sensorial |
3- Aula sistema sensorial |
|
4.1-Pêlo de U.Frey |
Material Biológico:
-Humano
Reagentes e Soluções:
-Água quente à 50 oC
-Água quente à 10 oC
-Álcool etílico
-Gelo Gelo triturado
Procedimentos:
1a. Etapa:
-Carimbar o colega no dorso da mão, na lateral do dedo indicador e na parte ventral do antebraço.
-Tomar 2 agulhas e mergulha-las por 5 minutos, uma em água a 50°C, e a outra em gelo triturado.
-Sem que o colega veja, pesquisar em algumas das zonas carimbadas os pontos sensíveis ao calor e ao frio.
-A cada estímulo pergunte ao colega qual sensação ele sentiu.
Obs.: Cuidar para que não fique nenhuma gota de água na ponta da agulha para não mascarar o resultado do experimento.
2a. Etapa:
-Colocar em uma bacia água a 50°C e em outra água a 10°C.
-Introduza o dedo indicador na água quente por 15 segundos ou o quanto resistir. Espere um pouco e introduza a mão inteira.
-Em qual experimento a sensação foi menos suportável? Introduza um dedo durante 15 segundos e após a mão inteira por outros 15 segundos, na bacia com água quente.
-Com a outra mão, na mesma bacia, introduza primeiro a mão inteira e depois o dedo, 15 segundos cada.
-Alternando a introdução do dedo e da mão, o que foi possível constatar?
-Repetir o experimento com a bacia com água fria.
-Compare as sensações que experimentou nos dois testes.
3a. Etapa:
-Preparar uma bacia com água a 10°C, outra com água a 50°C e bandeja com água a 33°C.
-Colocar simultaneamente uma das mão em água a 50°C e a outra mão na água a 10°C, durante 2 segundos.
-Após colocar ambas as mãos na bandeja com água a 33°C. Qual a sensação sentida em cada mão nas três temperaturas testadas?
4a. Etapa:
-Preparar um tubo de ensaio com gelo triturado, e outro água a 50°C.
-Aplicar sobre a fronte o tubo de ensaio com gelo durante 15 segundos.
-Anote o tempo de persistência da sensação de frio após a retirada do tubo.
-Repita o experimento deixando o tubo de ensaio com gelo durante um minuto.
-Anote novamente o tempo de persistência da sensação de frio após a retirada do tubo.
-Refaça o experimento com o mesmo colega, porém utilizando o tubo de ensaio com água a 50°C.
5a. Etapa:
-Colocar água quente (temperatura superior a 60°C) em dois beckers.
-Encoste um becker nos lábios e no outro introduza um dedo, simultaneamente.
-Em qual teste foi mais difícil resistir à temperatura?
6a. Etapa:
-Experimento com o pelo excitador de U. Frey (este pode ser construído colando um única cerda de pincel na extremidade de um palito de madeira).
-Explore o dorso da mão e a parte ventral do antebraço em busca de pontos de pressão, tato, frio ou qualquer outra sensação.
-Quais as sensações encontradas?
7a. Etapa:
-Assinale com uma caneta um ponto no dorso da mão do colega, sem que este o veja.
-A cada estímulo pergunte ao colega o que ele sentiu.
-Como foram as tentativas do colega? Próximas ou distantes?
-Repita o teste assinalando o ponto com mais pressão.
-Discuta os resultados.
8a. Etapa:
-Escreva com o dedo na testa do colega de olhos fechados, as letras b ou d, bem como, p ou q (ambas as letras devem ser minúsculas e "em forma").
-Qual a letra que o colega conseguiu identificar?
9a. Etapa:
-Com um compasso, com aberturas diferentes, pesquisar na lingua, dorso da mão, ponta do nariz, antebraço, nuca e face, a distância mínima em que o colega percebe claramente dois pontos estimulado.
-É necessário que as duas pontas do compasso sejam tocadas sobre o colega simultaneamente.
-Assinale os resultados na seguinte tabela, com um X quando o colega perceber os dois pontos, com uma + quando perceber apenas um ponto e 0 quando não houver percepção.
| Lingua | 5 cm | 3 cm | 2 cm | 1 cm | 0,5 cm |
| Dorso da mão | |||||
| Ponta do nariz | |||||
| Antebraço | |||||
| Nuca | |||||
| Face |
Observação: A partir da 2a. Etapa,utilize a seguinte tabela par quantificar as sensações do colega, em cada experimento.
| SENSAÇÕES | SIMBOLOGIA |
|
Morno Frio |
|
|
Quente Muito Frio |
|
|
Muito quente Frio congelante |
|
| Sensação Insuportável |
Análise dos Resultados:
Após a realização de todos os testes os alunos devem confrontar seus achados para reconhecer as variações de respostas possíveis entre os outros colegas de classe.
Discussão e Conclusões:
Após confrontar os resultados tentar explicá-los com base nos conceitos vistos durante as aulas teóricas.

REFELEXOS DE EQUILIBRIO
INTRODUÇÃO:
O aparelho vestibular é o órgão que detecta as sensações de equilíbrio. É composto por um sistema de tubos e câmaras ósseas o labirinto ósseo e, dentro deste, há um sistema de tubos e câmaras membranosas chamado de labirinto membranoso. É composto pela cóclea, três canais semicirculares e duas câmaras conhecidas como sáculo e utrículo. Os canais semicirculares, bem como o sáculo e utrículo são partes integrantes do mecanismo do equilíbrio.
OBJETIVOS:
Esta aula tem como objetivos: Estudo das seguintes propriedades do sistema de equilíbrio:
Sistema Vestibular: anatomia do labirinto; órgãos otolíticos; canais semicirculares; função; transdução e células sensoriais.
-Vias aferentes - eferentes.
-Adaptação - Habituação.
-Percepção vertical, movimento linear e rotatório.
-Movimento dos olhos.
- Papel vestibular no controle da postura:
Reflexos somáticos de orientação.
Reflexos visuais de orientação.
Lesões vestibulares.
Estudo das seguintes reações reflexas:
-Reflexo patelar.
-Reflexo aquileu.
-Reflexo plantar (reflexo de Babinski).
MATERIAL E MÉTODOS
1a Etapa: Sistema vestibular de cobaia.
Material Biológico:
-Cobaia.
-Reagentes e Equipamentos:
-Seringas descartáveis (3 ml). Xilocaína (2 %).
Procedimentos:
Injeta-se 2 ml de xilocaína no ouvido interno da cobaia, para a obtenção de nistagmo ocular e nistagmo de cabeça. Observar que nesta situação a cobaia tende a mover os olhos e pender a cabeça na direção do ouvido anestesiado.
Resultados: Qual o efeito do anestésico no ouvido da cobaia? Como este efeito é interpretado pelos receptores dos canais semicirculares?
2a Etapa: Ações Reflexas no Homem.
Material Biológico:
Homem.
Reagentes e Equipamentos:
-Assento rotatório.
-Venda para os olhos.
-Martelo neurológico. (1)
|
1.Martelo neurológico. |
Procedimentos:
1ª Etapa: Reflexos de Equilíbrio.
Colocar o colega no assento rotatório (não deixando o colega encostar os pés no chão). Procure que o colega fixe os olhos em um ponto. Gira-lo, não permitindo que ele mexa com a cabeça.
Colocar a venda nos olhos de um colega e fazer ele caminhar no corredor sem e com apoio. Como é o comportamento do colega ao ser guiado e ao ser deixado sozinho?
DISCUSSÃO DOS RESULTADOS:
A) Qual o efeito do anestésico no ouvido do cobaio? Comparando com o cobaio que recebeu o anestésico com seu controle, quais as diferenças?Por quê?
B) O que você observou nos olhos do colega? Explique. C) Qual a diferença entre a marcha cega sem apoio e com apoio? Por que e explique.
CONCLUSÕES .

PRESSÃO SANGÜÍNEA ARTERIAL NO HOMEM
INTRODUÇÃO
O bombeamento cardíaco é responsável pela produção de pressão no sistema circulatório. Durante sua fase sistólica o coração normal de um jovem adulto exerce uma pressão de 120 mm Hg nos vasos aórticos. Já na fase diastólica, quando o músculo inicia seu relaxamento, a máxima pressão exercida é de 80 mm Hg. A determinação da pressão sangüínea constitui parte do padrão universal do exame físico. É com base nela que elaboram-se muitos diagnósticos, concedem-se ou recusam-se seguros de vida, fazem-se prognósticos, e avalia-se o tratamento.
OBJETIVOS: Determinar a pressão sangüínea arterial (PSA) no homem, mediante método indireto, em distintas situações. Verificar a frequência cardíaca através do pulso radial.
MATERIAL:
Material Biológico:
-Homem
Equipamentos:
-Colchão (1)
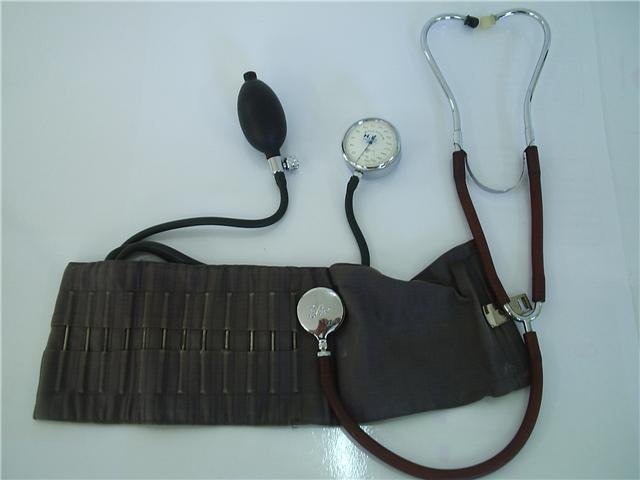
-Esfignomanômetro (2)
-Estetoscópio (2)
-Manguito (2)
|
1.Colchão |
2- Estetoscópio, esfignomanômetro |
PROCEDIMENTOS
1a Etapa:
-Determinar a PSA nas posições sentado, deitado, em pé e após a realização de exercício (ex.: correr durante alguns minutos).
-Posicionar o manguito na parte superior do braço;
-O estetoscópio deve ser posicionado no antebraço sobre a artéria antecubital;
-Sem insuflar o manguito tente verificar a existência de algum som ou ruído.
-Obstruir a artéria braquial insuflando o manguito;
-Após insuflar o manguito tente verificar a existência de algum som ou ruído.
-Diminuir gradualmente a pressão do manguito;
Atenção: Ler no manômetro a pressão equivalente ao primeiro som de batida (SISTÓLICA) e ao primeiro som grave (DIASTÓLICA).
2a Etapa:
-Determinar a frequência cardíaca através do pulso radial nas posições sentado, deitado, em pé e após a realização de exercício (ex.: correr durante alguns minutos).
DISCUSSÕES E CONCLUSÕES
Fazer a estatística básica e comparar os resultados entre os colegas.

PNEUMOGRAFIA NO HOMEM
INTRODUÇÃO
A ventilação pulmonar consiste na inspiração e expiração. A inspiração promove a entrada de ar nos pulmões, e dá-se pela contração da musculatura do diafragma e dos músculos intercostais. O diafragma abaixa e as costelas elevam-se, promovendo o aumento da caixa torácica, com consequente redução da pressão interna em relação à externa, forçando o ar a entrar nos pulmões. A expiração promove a saída de ar dos pulmões, e dá-se pelo relaxamento da musculatura do diafragma e dos músculos intercostais. O diafragma eleva-se e as costelas abaixam, o que diminui o volume da caixa torácica, com consequente aumento da pressão interna, forçando o ar a sair dos pulmões.
1. OBJETIVO: Verificar o ritmo respiratório humano e os efeitos de fatores que interferem no ritmo normal.
2. MATERIAIS:
A) Material biológico:
- Humano.
B) Equipamento:
- Pneumógrafo com válvula de Verdin (1);
- Quimógrafo (1, 2);
- Tambor de Marey (3.1 e 3.2);
- Copo com água.
|
1.Pneumógrafo com válvula de Verdin |
2.Quimógrafo |
|
3.1.Tambor de Marey |
3. PROCEDIMENTOS
Coloque o pneumógrafo ao redor do tórax do aluno na região supradiafragmática (se for feminino, o pneumógrafo deverá ser colocado na parte superior do tórax ).
3.1. RITMO NORMAL DA RESPIRAÇÃO. Fazer um registro da respiração normal em posição sentada por 15 seg. OBS.: O aluno deverá respirar normalmente. Observar o gráfico e indicar as fases da respiração no gráfico.
3.2. FATORES QUE INTERFEREM NO RITMO RESPIRATÓRIO.
Fazer registro do ritmo respiratório nas seguintes posições: deitado, sentado e de pé (seguindo essa ordem), por um minuto em cada posição. Repetir a experiência com outros componentes do grupo e comparar os resultados. Observar o gráfico e comparar as freqüências.
3.3. INIBIÇÃO DA RESPIRAÇÃO.
Fazer um traçado da respiração normal durante 15 seg. Após, o aluno deverá beber um copo com água sem parar, continuando o traçado por 15 seg. Observar o gráfico e indicar as fases da respiração no gráfico.
3.4. EFEITO DO EXERCÍCIO SOBRE A RESPIRAÇÃO. Fazer um traçado da respiração normal durante 15 seg. Desconectar o pneumógrafo do quimógrafo. O aluno deverá correr com o pneumógrafo no tórax durante 2 minutos, fora do laboratório. Conectar o pneumógrafo e registrar logo após o exercício, o ritmo respiratório por 15 seg. na posição sentado. Comparar o ritmo respiratório e contar a frequência antes e após o exercício.

ÓPITCA FISIÓLOGICA
INTRODUÇÃO Óptica fisiológica é o ramo da Óptica que estuda as características físicas, biológicas e ambientais do olho e como estas influenciam nos tratamentos utilizados em pacientes com defeitos visuais. 1.
OBJETIVOS: Estudar aspectos da óptica fisiológica no olho humano, de rã e em modelo óptico.
2. MATERIAL:
A) Material biológico:
- Humano
- Rã
B) Soluções e equipamentos:
- Água destilada; - Uretana a 10% - 2 ml / 50g de rã;
- Tabuleta de Mariotte (1);
- Tábua de Snellen; quadro comluz e letras - Tábua de Ishihara (2.1 e 2.2);
- Perímetro (3.1 e 3.2);
- Olftalmoscópio (4);
- Modelo de olho (5);
- Olho artificial (6.1, 6.2 e 6.3)
- Gases;
- Lápis.
3. PROCEDIMENTOS:
A) OFTALMOSCOPIA:
Após aprender a usar o olftalmoscópio, fazer o exame de olho, no olho artificial, olho da rã e no olho do colega. No olho do colega fazer o paciente olhar na direção da orelha do observador do mesmo lado do olho observado e acomodar a visão a distância infinita; há relaxamento do músculo ciliar e do esfíncter da íris. Tentar visualizar com o olftalmoscópio a mácula lútea com a fóvea centralis, no olho artificial e no do colega.
B ) PONTO CEGO: Para comprovar a existência do ponto cego, ou papila óptica, proceder da seguinte maneira: fechar o olho direito, manter a tabuleta cerca de 15cm à frente do olho esquerdo e olhar fixamente para o disco. Mover lentamente a tabuleta em direção ao olho até que a cruz desapareça.
C) ACUIDADE VISUAL:
Fazer o exame de acuidade utilizando a tábua de Snellen. Para tal o aluno deverá ficar a 6m de distância da tábua.
D) VISÃO DAS CORES:
Fazer o teste para visão das cores com a tábua de Ishihara.
E) PERIMETRIA: Com o perímetro determinar o campo visual para o branco, verde e vermelho.
F) MODELO DE OLHO:
Com o modelo de olho artificial proceda o seguinte roteiro:
a) Olho normal: - Pantalha em 11. - Lente +20 no 6. - Lâmpada a 35 cm de distância. - Focar na mácula e, após no ponto cego. - Observar a inversão da imagem, usar a Íris.
b) Hipermetropia: - Pantalha em 10. - Lente +20 no 6. - Aumentar a distância da lâmpada até obter a imagem clara. - Correção com lente +2 em 1.
c) Miopia : - Pantalha em 12. - O resto igual ao número 1. - Correção com lente -1.75 em 1.
d) Astigmatismo : - Pantalha em 11. - Lente +20 no 6. - Lâmpada a 35 cm. - Lenta -5.50 em 4 e + 1.75 em 1.
e) Acomodação: - Retirar lente +20. - Pantalha em 11. - Lente +7 em 4. - Focar objeto distante , panorama observado de uma janela.
f) Remoção do cristalino: - retirar o cristalino e por +7 em 2 a 20cm lâmpada
g) Uso de óculos por pessoa com olhos normais: - Pantalha 11. - Cristalino +20 em 6, distância da lâmpada 35cm (a imagem se projeta nítida) por lente +2 em 1 e a imagem foca borrada (observar desenho).
4. DISCUSSÃO DOS RESULTADOS
5. CONCLUSÕES
|
1- Tábua de Mariotte |
2.1- Tábua de Ishihara |
|
|
3.1- Perímetro |
4- Oftalmoscópio |
|
|
5- Modelo de olho em cortes |
6.1- Olho artificial |
|
|
6.2- Parte do olho artificial |
6.3- Parte do olho artificial |

ESTUDO DO NERVO E DA PLACA MOTORA
INTRODUÇÃO : Uma junção neuromuscular é a junção entre a parte terminal de um axônio motor com uma placa motora, que é a região da membrana plasmática de uma fibra muscular (o sarcolema) onde se dá o encontro entre o nervo e o músculo permitindo desencadear a contração muscular. Na junção neuromuscular o neurotrasmissor utilizado é a acetilcolina. A fibra nervosa ramifica-se no final, para formar a placa terminal, que se invagina para dentro da fibra muscular, mas repousa inteiramente na parte externa da membrana.
OBJETIVOS: Esta aula objetiva estudar as propriedades dos nervos e suas conexões com os tecidos musculares, os potenciais de repouso e de ação, a lei da integridade do nervo e a excitabilidade nervosa.
MATERIAL:
A) Material biológico:
- Rã (Rana sp.).
B) Reagentes e equipamentos:
- Estimulador (1)
- Material cirúrgico e linhas.
- Seringa ( 3 ml ).
- Cloreto de sódio.
- Lamparina.
- Pistola de Dubois
– Reymond (2).
- Flaxedil.
- Vidro de relógio.
- Ringer.
|
1- Estimulador |
2. Pistola de Dubois |
PROCEDIMENTOS CIRÚRGICOS:
A) TRANSMISSÃO NEURO - MUSCULAR. AÇÃO DO CURARE.
1.Destrua o sistema nervoso central do animal.
2.Segure a rã com a mão esquerda, flexionando a cabeça com o indicador;
3.Localize a articulação atlo-occipital, situada no centro da linha imaginária que tangencia o bordo inferior da mancha timpânica;
4.Seccione a medula com um bisturi;
5.Introduza o estilete (sentido caudal) no canal medular e gire o estilete várias vezes para destruir toda a medula ;
6.Dirija a ponta do estilete cranialmente e, com movimentos de lateralidade destrua o encéfalo. O animal ficará completamente imóvel;
7.Isole os dois nervos ciáticos , sem tirar completamente a pele da região para manter o saco linfático dorsal;
8.Faça uma ligadura numa das patas deixando livre o nervo ciático correspondente (observar o desenho);
PROCEDIMENTOS EXPERIMENTAIS:
1- Estimular, isoladamente, o nervo ciático e o músculo gastrocnêmio de ambas as patas;
2- Injetar 2 ml de Flaxedil (galamina ) no saco linfático dorsal e esperar 60 minutos;
3. Excitar com estímulo isolado o nervo da pata com a ligadura e depois o músculo;
4- Excitar com estímulo isolado o nervo da pata sem a ligadura e depois o músculo.
B) POTENCIAL DE REPOUSO E POTENCIAL DE AÇÃO.
1- Preparação do animal: A rã é imobilizada por destruição do sistema nervoso central que é feita igual ao experimento anterior.
2- Preparação da pata galvanoscópica : Pata galvanoscópica, como o nome indica, compreende uma pata posterior da rã, escorchada, seccionada acima do joelho e que conserva o nervo ciático tão longo quanto possível.
1.Após a destruição do SNC da rã, coloca-se sobre uma placa de cortiça e faz-se uma incisão circular da pele em redor da coxa.
2.Mantém-se com a mão esquerda o segmento anterior do animal e arranca-se, com auxílio de uma pinça-dente-de-rato na mão direita, a pele dos membros posteriores da rã.
3.Retira-se a pele com uma tração vigorosa, mas com cuidado, destacando as aderências quando necessárias.
4.Destaca-se por meio de pinça e tesoura as aderências da pele com o ânus, retirando-se toda a pele até a altura dos membros anteriores.
NOTA IMPORTANTE: O tecido muscular exposto pela retirada da pele não deverá entrar em contato com a superfície externa da pele ou mesmo com o local onde esta estava tocando. Isto porque a superfície externa da pele secreta substâncias que são tóxicas aos tecidos internos e que podem tornar o músculo impróprio para as experiências. Portanto, uma vez retirada a pele deve-se trocar a placa. Deve-se também manter o tecido exposto constantemente umedecido com a solução de Ringer, para evitar que se torne seco.
Procede-se agora a dissecação do ciático em todo o comprimento, desde a articulação do joelho até a bacia, ao nível das raízes pelos quais emergem do canal raquidiano.
1.Para isso deita-se a rã sobre o ventre, de maneira que fique exposta a face posterior da coxa escorchada;
1.Percebem-se dois interstícios musculares longitudinais, um externo que separa o vasto externo do tríceps, do bíceps femoral, e um interno que separa o bíceps do semi-membranoso.
2.No fundo deste interstício interno, entre o bíceps e o semi-membranoso encontram-se o nervo ciático e os femorais .
3.Com os dois bastões de vidro pontiagudos, procede-se o afastamento dos músculos e isola-se o ciático na maior extensão possível.
NOTA IMPORTANTE: Não esquecer que o nervo não deve ser tocado com instrumentos metálicos. É preciso dissecar com grande cuidado, para evitar trações nocivas.
1.Para subir a dissecação até as origens do nervo (raízes raquidianas 7a, 8a, 9a ), tomam-se como referência, na região pélvica os dois ossos ilíacos e, no meio do seu intervalo, a 10a vértebra cóccix (na rã = hipostilo).
1.Com uma pinça levanta-se a extremidade posterior desta vértebra e, por meio de uma tesoura reta, secionam-se os músculos periformes e ileococcigeos, incisando os tegumentos em toda a espessura, sempre paralelo ao osso até a sua articulação com a 9a vértebra.
2.Rebate-se o hipostilo e, com uma tesoura corta-se ao nível da base. Deve-se ter a preocupação, nesta preparação, de não lesar os grandes vasos subjacentes ao osso: aorta abdominal e seus dois ramos de bifurcação (ilíacas).
3.Percebe-se então, além destes vasos, a direita e a esquerda, três filetes nervosos convergentes para baixo, que são as raízes dos ciáticos .
4.Ainda com bastões de vidro, disseca-se um dos grupos de raízes e. por baixo, passa-se um fio e atasse um nó, o mais alto possível. Toda a pata é sacudida por um forte abalo, que nasce em conseqüência da excitação mecânica do nervo. Repete-se o procedimento com a outra pata.
5.Secciona-se acima da ligadura e, exercendo uma leve tração sobre o segmento distal do nervo, por meio do fio, completa-se o isolamento até a extremidade inferior da coxa.
6.Rebate-se o nervo sobre a perna, aplica-se a superfície do gastrocnêmio e separa-se a perna da coxa por uma seção transversal praticada um pouco acima do joelho.
7.Colocar as patas galvanoscópicas numa superfície limpa e seca, cuidando sempre para manter úmido de Ringer a musculatura e o nervo ciático.
6. PROCEDIMENTOS EXPERIMENTAIS:
a. Observar o potencial de repouso: Pega-se uma pata galvanoscópica (pata A) e coloca-se o nervo de modo que um ponto toque numa parte integra do tecido e outra numa porção lesada. Observar.
b. Observar o potencial de ação:
- Colocar o ciático em alça da pata "A "sobre o gastrocnêmio da outra pata galvanoscópica (pata B ).
- Excitar com estímulo elétrico o isquiático da pata " B ". Observar.
C) LEI DA INTEGRIDADE DO NERVO - PISTOLA DE DUBOIS - REYMOND.
A pistola de Dubois - Reymond consta de três eletrodos metálicos: o eletrodo do centro é de zinco, os outros dois são de cobre. Cada eletrodo comunica-se com o interruptor da pistola, que permite estabelecer contato dos mesmos aos pares.
PROCEDIMENTOS EXPERIMENTAIS:
a. Colocar o nervo isquiático preparado previamente (pata galvanoscópica A) em relação com os três eletrodos;
b. Observar o desenho;
c) Apertar o interruptor que estabelece o contato do eletrodo número 1 de cobre mais próximo ao músculo com o número 2 de zinco. Depois proceder da mesma maneira, estabelecendo o contato do eletrodo número 3 de cobre e número 2 de zinco. Observar;
d. Passar um fio de linha sob o nervo, exatamente entre o eletrodo número 1 e o eletrodo número 2 de zinco. Apertar o interruptor que estabelece o contato dos eletrodos que ficam acima da ligadura (2 e 3 ). Observar;
e) Com um corte separar perfeitamente as duas extremidades do nervo ao nível da ligadura de tal modo que se suprima toda a continuidade física . Apertam-se os dois interruptores separadamente. Observar;
f) Restabelecer a continuidade física do nervo, pondo as duas extremidades em contato, pressionando-se sobre o interruptor que estabelece contato entre o eletrodo número 1 e número 2. Observar.
D) EXCITABILIDADE DO NERVO.
No interesse de utilizar a mesma preparação para os diversos estímulos , estes serão experimentados na ordem do que menos lesa ao mais lesivo, isto é, excitante elétrico, térmico, mecânico e químico. Será realizada na outra pata galvanoscópica
(B). PROCEDIMENTOS EXPERIMENTAIS:
a. Excitante elétrico: estimular com o estimulador Harvard. Observar.
b. Excitante térmico: tocar o nervo da preparação com o estilete aquecido na sua porção mais distal. Observar.
c. Excitante mecânico: já na preparação da pata, ficou evidenciada a ação mecânica de uma ligadura feita na extremidade superior do isquiático. Observar.
d. Excitante químico: colocar NaCl num vidro de relógio e colocar a extremidade livre do isquiático da pata galvanoscópica. Observar.

REGULAÇÃO DA RESPIRAÇÃO NO CÃO
Introdução: Do ponto de vista da fisiologia, respiração é o processo pelo qual um organismo vivo troca oxigênio e dióxido de carbono com o meio ambiente. O oxigênio é necessário para a respiração celular, enquanto que o dióxido de carbono é um sub-produto do metabolismo e deve ser retirado do organismo. Nos vertebrados terrestres, as trocas gasosas da respiração realizam-se em órgãos denominados pulmões. A entrada e saída do ar – com composição diferente, devido às referidas trocas gasosas – é provocada pelos movimentos (geralmente involuntários) dos músculos do tórax.
Objetivo: Demonstrar os vários fatores que influem na regulação da respiração.
Material biológico: cão
Material procedimental:
- pneumógrafo
- quimógrafo
- saco plástico
- tubo de borracha
- bomba de respiração artificial
- estimulador
- seringa
- nanômetro de PSA - linha
Soluções:
•Na2Co3 – 10%
•Ácido lático – 10%
•Soro fisiológico – 9%
Procedimentos:
1.Preparação do animal
1.1.Anestesiar com Nembutal o cão com 10% a 15% menos que o recomendado (30mg/quilo de peso)
1.2.Isolar as seguintes estruturas:
- as artérias carótidas
- os nervos vagos
- a traquéia
- a veia jugular externa para colocação da cânula de polietileno
- a artéria femoral para a colocação do manômetro de PSA.
- a veia jugular para a colocação do soro
- a veia femural para a colocação da cânula de polietileno para injetar as soluções
1.3. Instalar o pneumógrafo.
Experimentação – Fatores que influem na regulação da respiração.
•EXPERIÊNCIA DE BARRY: Introduzir na veia jugular externa, em direção ao coração, uma cânula de polietileno cheio de T 1824 (Anil de Evans) e verificar a aspiração torácica durante a inspiração. A cânula deve ser fixada com um fio de linha assim como amarrada a porção mais distal da veia.
•Registro da respiração do animal
•Diminuição do espaço morto: Traqueostomia
•Aumento do espaço morto: Colocar a cânula traqueal e unir ao tubo bomba de respiração artificial desligada ou a um simples tubo.
•Ação do CO2: Adaptar na cânula traqueal com um saco plástico deixando o animal respirar seu próprio ar expirado.
•Equilíbrio ácido-básico
- injetar devagar na veia femoral, através de cânula de polietileno ácido lático a 10% de 5 a 10 ml, logo em seguida injetar 2 ml de soro fisiológico.
- injetar na veia femoral, através da cânula de polietileno Na2CO3 a 10% de 5 a 10 ml, logo em seguida injetar 2 ml de soro fisiológico.
ATENÇÃO: Entre um e outro experimento esperar que a respiração do animal retorne ao ritmo normal.
•Colocar a bomba de respiração artificial e abrir o tórax do animal
- Observar os pulmões
- Cortar os vagos, e após estimular os cabos centrais, no início da inspiração (reflexo de Hering-Brauer).
- Desligar a bomba de respiração artificial – Pneumotórax.

OSMOREGULAÇÃO
Introdução: Os fluidos corporais dos poliquetas são hiperosmóticos com relação ao meio e o influxo de água promove diferenças na sua concentração osmótica, isto é, o animal que apresenta seus fluídos hiperosmóticos em relação ao meio tende a absorver água e incha aumentando o seu peso. O decréscimo do peso significa que o animal é capaz de excretar alguma água e/ou gerar mudanças na sua permeabilidade corporal e/ou através da perda de sais.
Objetivo: Demonstrar as dificuldades encontradas pelos animais que se encontram em um meio hiposmótico. Material biológico: Poliqueta estuarino Laeonereis acuta
Material procedimental:
- água marinha 10 ppm (grupo 1)
- água destilada (grupo 2)
- água do mar e destilada em partes iguais (grupo 3)
- água do mar e sacarose isosmótica em partes iguais (grupo 4)
- sacarose osmoticamente equivalente a água do mar (grupo 5)
Procedimentos:
1.Cada grupo determinará o peso inicial dos animais que estão na água do mar;
2.Os animais serão transferidos para as soluções descritas anteriormente (cada grupo trabalhará com uma solução);
3.A determinação do peso será realizada a cada 15 minutos em um intervalo de 90 minutos;
4.Ao final desse período, todos os animais serão colocados novamente na água do mar e a determinação do peso será efetuada a cada 15 minutos durante 60 minutos.

FISIOLOGIA DO CORAÇÃO NEUROGÊNICO
Objetivos: Determinar os efeitos de neurotransmissores no coração neurogênico de invertebrados.
Material biológico: Espécie preferencialmente grande de Brachyura.
Materiais procedimentais:
| Acetilcolina = 0,01 mg/ml | Adrenalina = 0,1 mg/ml | Serotonina = 0,1 mg/ml |
| Material cirúrgico |
Vidraria comum de laboratório |
Procedimentos cirúrgicos:
1.Amarre o animal em uma placa e coloque-o em uma bacia com água do mar. → O dorso do animal deve permanecer exposto.
2.Exponha o coração do animal abrindo a região cardíaca uma pequena janela. → Para tanto raspe a carapaça ao longo das linhas que delimitam a região cardíaca e retire-a cuidadosamente.
Procedimentos experimentais:
1. Observe o coração pulsando e registre a freqüência cardíaca.
2. Goteje diretamente sobre o coração serotonina, adrenalina e acetilcolina.
3.Lave o coração com água do mar entre a administração de cada droga.
4.Registre a freqüência cardíaca enquanto o coração estiver sobre o efeito de cada uma das drogas, bem como a temperatura.

FISIOLOGIA DO CORAÇÃO MIÔGENICO
Objetivos: Determinar os efeitos de neurotransmissores no coração miogênico de vertebrados inferiores.
Material biológico: Espécie de teleósteo ou anfíbio.
Material procedimental:
|
Solução fisiológica para teleósteo ou anfíbio |
Material cirúrgico |
| Acetilcolina = 0,1 mg/ml | Vidraria comum de laboratório |
| Adrenalina = 0,1 mg/ml | Quimógrafo e acessórios (1.1 e 1.2) |

Procedimentos cirúrgicos:
1.Espinhale o animal e fixe-o em decúbito dorsal.
2.Exponha o coração.
3.Prenda-o a alavanca do Quimógrafo, fixando a extremidade do ventrículo ao fio que conduz a mesma.
Procedimentos experimentais:
1.Controle cuidadosamente a tensão exercida sobre o coração. Procure colocar a alavanca na horizontal e o fio o mais p erpendicular possível à mesma.
2.Coloque um cilindro enfumaçado (1.1) na base do Quimógrafo (1.2) e aproxime-o da alavanca.
3.Registre a freqüência cardíaca normal durante alguns minutos e pare o cilindro.
4.Goteje adrenalina diretamente sobre o coração e repita o registro.
5.Lave a preparação abundantemente com solução fisiológica (cilindro preparado).
6.Goteje Acetilcolina diretamente sobre o coração e repita o registro. Discussão sugerida: Descreva a regulação nervosa da atividade cardíaca nas diferentes classes de invertebrados.


DETERMINAÇÃO DA CONCENTRAÇÃO DE AMÔNIA NA ÁGUA
Introdução: O íon de amônia resulta da mineralização do nitrogênio. O nitrogênio ligado organicamente nos restos de comida e nos excrementos é transformado pelas bactérias que separam albumina, sendo libertado sob a forma de ions inorgânicos de amônio NH4+ e amoníaco NH3-. O amônio é muito perigoso na medida em que afeta severamente o processo respiratório. Penetra facilmente nas células, fazendo subir o pH e bloqueando as funções vitais.
Objetivos: Determinar a concentração total de amônia na água Na quantificação da amônia total, será utilizado um eletrodo de amônia.
O pH das amostras de água é aumentado, utilizando uma solução ISA (5 M de NaOH, 0,5 M de EDTA dissódico e 1% de indicador de pH). Os passos a serem seguidos são:
1.Fixar a leitura do aparelho à -10 mV, utilizando 50 ml de água, na qual foi adicionado 1 ml de solução ISA. A leitura deve ser realizada sob agitação constante, com o becker tapado.
2.Realizar a reta padrão, uma por cada salinidade ensaiada. A 50 ml da mesma água utilizada nos ensaios, adicionar distintas quantidades de soluções padrão de amônia, segundo o detalhado na tabela:
| Concentração final | Quantidade de água |
Quantidade de solução padrão |
Quantidade de solução ISA |
| 10 -5 M | 50 ml |
1 ml de uma solução de 10-3 M de amonia |
1ml |
| 10-4 M | 50 ml |
50 µl de uma solução 0,1 M de amônia |
1ml |
| 10-3 M | 50 ml |
0,5 ml de uma solução de 0,1 M de amônia |
1ml |
| 10-2 M | 50 ml |
5 ml de uma solução de 0,1 de amônia |
1ml |
3. A 50 ml de amostra de água utilizada nos ensaios com os animais, adicionar 1 ml de solução ISA e registrar a diferença de potencial (Em mV) IMPORTANTE: A solução ISA é extremamente cáustica. Manipular com cuidado e não despejar pela pia.

COLETA DE SANGUE DE RATO POR EXSANGUINAÇÃO
Objetivo: Obter sangue de ratos por exsanguinação, para ser utilizado em experimentos.
Cada rato adulto fornece aproximadamente 10 ml. As quantidades especificadas são para um total de 50 ml de sangue
Material biológico: 5 ratos adultos
Material procedimental:
|
solução de uretana em água destilada,100 mg/ml |
Tesoura para pele |
| Balança para pesar ratos |
5 conjuntos de seringa de vidro de 10 ml com agulha 25 X 8 |
|
seringa e agulha para injeção intraperitonial |
1 ampola de heparina (Liquemine Roche), 0,25 ml=5000 U.I. |
| suporte para rato anestesiado | Solução Ringer ou NaCl 9 g/l |
| Algodão | 1 béquer de aprox. 20 ml |
| Pinça com dentes para pele | proveta ou erlenmeyer de 50 ml |
Procedimentos:
3.Colocar o rato no suporte.
4.Molhar com água os pelos do abdome. Abrir o abdome por uma incisão mediana, utilizando a pinça e a tesoura.
5.Afastar as vísceras abdominais para a direita do animal, expondo a gordura retroperitonial, atrás da qual se encontra a aorta.
6.Expor a aorta retirando a gordura retroperitonial com algodão seco.
7.Puncionar a aorta com a seringa dotada da agulha 25 X 8 e injetar a solução de heparina que nela foi colocada.
8.Extrair o sangue. Será obtido um volume de 10 ml, aproximadamente.
9.Retirar a agulha da seringa e colocar o sangue na proveta (ou erlenmeyer).
10. Lavar com água imediatamente a seringa e a agulha utilizadas.

CONSUMO DE OXIGÊNIO EM ANIMAIS TERRESTRES
Objetivos: Avaliar o consumo de oxigênio e a taxa metabólica em diferentes grupos de animais.
| Material biológico: | Material procedimental: |
|
PARTE A – Brachyura de respiração aérea |
- Absorvente de CO2 |
|
PARTE B – Pequena rã ou camundongo |
- Respirômetro de Krogh (1-desenho do Euclydes) |

Procedimentos:
1.Monte o respirômetro.
3.Fechar o aparelho
4.Marcar o nível do líquido no manômetro (2) e a posição do êmbolo na seringa
7.Não esqueça de registrar a temperatura.

ABALO E TÉTANO - MÚSCULO ERGOGRAFIA
Objetivos: Determinar os efeitos de Abalo, Tétano e Fadiga no músculo de Rana sp.
Material biológico: Rã (Rana sp.)
Material procedimental:
|
Ringer (solução fisiológica para anfíbios ). |
Estimulador |
| Quimógrafo e acessórios (1.1 e 1.2) | Miógrafo |
| Material cirúrgico | Eletrodos |

Cilindro Esfumaçado
Procedimentos cirúrgicos:
1.Utiliza-se uma rã;
2.Imobilize – a;
3.Após imobilizado, faça uma incisão circular na pele do animal, ao redor da coxa e retire-a;
4.Lavar as mãos após a retirada da pele para não alterar a preparação;
5.Mediante incisão dorsal paralela coluna vertebral desde a extremidade final do urostilo, isole cuidadosamente o nervo ciático com o auxílio de bastões de vidro pontiagudos;
6.Amarre um fio de linha na sua porção mais cranial e seccione acima da ligadura;
7.Seccione a extremidade distal do tendão de Aquiles e isole o gastrocnêmio;
8.Mantenha a extremidade superior do músculo ligada a extremidade inferior do fêmur;
9.Corte o fêmur, retire a tíbia e coloque a preparação numa placa de petri com Ringer por alguns minutos;
10.Tocar dois pontos do nervo e do músculo com uma pinça de Galvani para verificar se a preparação foi corretamente executada;
11.Montar o gastrocnêmio fixando-o pelo fêmur a uma pinça femura;
12.Pelo tendão liga-lo a alavanca muscular;
13.Repousar o nervo sobre as extremidades do eletrodo estimulador tomando o cuidado de mantê-lo umedecido;
14.Colocar logo abaixo um sinal elétrico de Deprez para registrar no cilindro o momento em que for dado o estímulo.
Procedimentos experimentais: Colocar o quimógrafo em funcionamento e executar cada um dos seguintes experimentos:
a) Abalo. Estimular o nervo com estimulo supra-liminar simples e observar.
b) Tétano. Estimular o nervo com estimulo supra-liminar repetitivo e observar.
c) Fadiga. Manter a estimulação tetânica e verificar que o músculo, após certo tempo, para sua contração. No entanto, se estimularmos o músculo diretamente, não via nervo, ele o fará? Por quê?

Suporte do Quimógrafo
Retire o papel do cilindro e feixe - o com goma-laca. Não se esqueça de anotar no papel, antes de fixá-lo, o título de experimento, data, temperatura, intervalo de tempo e o seu nome. A intensidade com que o músculo foi estimulado, bem como a freqüência por ocasião do tétano, devem estar registrados em seu caderno.
Excitabilidade do nervo: Será realizada na outra pata galvanoscópica .
No interesse de utilizar a mesma preparação para os diversos estímulos, estes serão experimentados na ordem do que menos lesa ao mais lesivo, isto é, excitante elétrico, térmico, mecânico e químico.
a) Excitante elétrico - estimular com o estimulador Harvard. →Observar.
b) Excitante térmico - tocar o nervo da preparação com o estilete aquecido na sua porção mais distal. →Observar.
c) Excitante mecânico - já na preparação da pata, ficou evidenciada a ação mecânica de uma ligadura na extremidade superior do isquiático. →Observar.
d) Excitante químico - colocar NaCl em um vidro de relógio e colocar a extremidade livre do isquiático da pata galvanoscópica. →Observar.